Công ty cổ phần công nghệ sinh học dược Nanogen đã có văn bản kiến nghị Thủ tướng về việc xin cấp phép khẩn cấp cho vắc xin Nanocovax.
Đại diện Công ty cổ phần công nghệ sinh học dược Nanogen (Khu công nghệ cao TP.HCM), 1 trong 4 đơn vị sản xuất vắc xin ngừa COVID-19 của Việt Nam, cho biết họ vừa có văn bản kiến nghị Thủ tướng xin cấp phép khẩn cấp cho vắc xin Nanocovax.
Theo đại diện Nanogen, dựa trên các kết quả thử nghiệm lâm sàng, khả năng sinh miễn dịch của vắc xin Nanocovax đạt 99,4%, nếu so sánh với các loại vắc xin khác trên thế giới thì không hề thua kém và có phần cao hơn.
Nanogen cho biết giá bán dự kiến Nanocovax đang thấp nhất thế giới, chỉ với 120.000 đồng/liều.
"Đến nay công suất sản xuất của nhà máy Nanogen ước đạt 8-12 triệu liều/tháng. Chúng tôi đang hoàn thiện, mở rộng hệ thống kho lạnh với sức chứa 10 triệu liều cũng như đội ngũ xe lạnh (2-8°C) vận hành đạt chuẩn quốc tế. Dựa trên kế hoạch và năng lực hiện tại, chúng tôi dự kiến cung cấp đủ 50 triệu liều đến tháng 12.2021 và 100 triệu liều vào năm 2022", đại diện Nanogen cho hay.
Với các điều kiện nêu trên, Nanogen kiến nghị Chính phủ để vắc xin Nanocovax sớm được cấp phép khẩn cấp có điều kiện, tương tự như các loại vắc xin của Nga (Sputnik V), Trung Quốc (Sinopharm) và Mỹ (Pfizer).
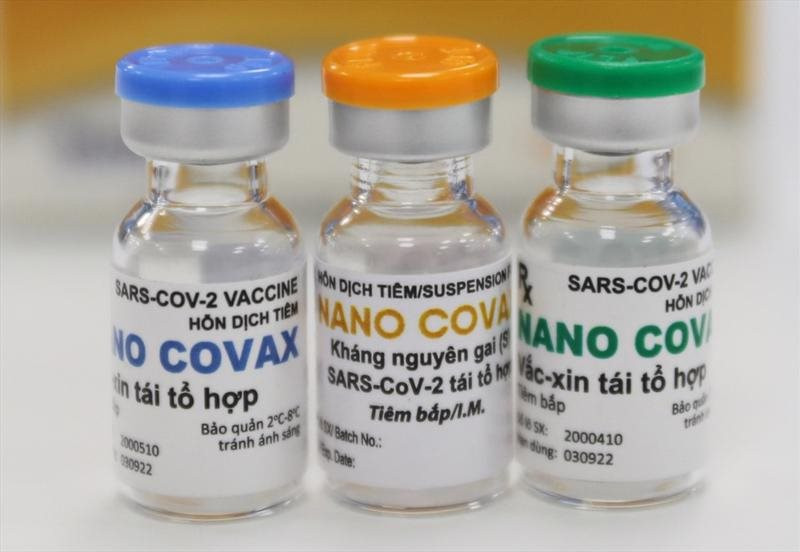
Nanocovax là loại vắc xin COVID-19 do Nanogen nghiên cứu và phát triển từ tháng 5.2020, dựa trên công nghệ protein tái tổ hợp.
Nanocovax vừa kết thúc thử nghiệm lâm sàng giai đoạn 1 và 2, được Hội đồng đạo đức Bộ Y tế đánh giá tốt và đã thông qua đề cương nghiên cứu, triển khai thử nghiệm lâm sàng giai đoạn 3 trên quy mô 13.000 người. 13.000 tình nguyện viên tham gia giai đoạn 3 có độ tuổi 18-75, chỉ cần kiểm tra công thức máu và kiểm tra kháng thể với SARS-CoV-2.
Ngày 11.6, Bộ Y tế đã quyết định phê duyệt đề cương nghiên cứu thử nghiệm lâm sàng giai đoạn 3 của vắc xin Nanocovax. Việc thử nghiệm này được tổ chức tại Học viện Quân y, tỉnh Hưng Yên, Viện Pasteur TP.HCM, tỉnh Long An, tỉnh Tiền Giang và một số đơn vị đủ điều kiện theo quy định tại các tỉnh triển khai nghiên cứu.
Tính đến sáng 22.6, các đơn vị nghiên cứu đã hoàn thành thử nghiệm 1.000 mũi tiêm đầu tiên, liều 25mcg (liều duy nhất, tỉ lệ tiêm 6:1, tức 6 người tiêm vắc xin, 1 người tiêm giả dược). Sau tiêm, các tình nguyện viên có sức khỏe ổn định.